【案例分享】MCM CulMsc-SFM31 Pro培养基突破MSC大规模培养瓶颈,赋能临床级细胞高效量产
- 2025-11-28
- 新闻资讯
- 537

间充质干细胞(MSC)凭借自我更新能力、多向分化潜能(成脂、成骨、成软骨)及强大的免疫调节作用,已成为再生医学与个性化医疗领域的 “种子细胞”。其中,脐带来源 MSC 因免疫原性低、取材无创、易扩增的优势,在临床试验中占据主导地位。
但临床应用对MSC 的需求量极高——单次回输需约1E10细胞,且需多次给药,“规模化量产” 与 “质量稳定” 的双重挑战,成为制约MSC疗法落地的关键。今天,我们就为大家拆解一套经过实战验证的MSC大规模培养解决方案,助力科研团队高效推进临床转化。
相较于传统二维培养,三维培养虽能模拟体内生理微环境,提升细胞活力与功能,但实际操作中,两大痛点常让科研团队“卡壳”:
(1)量产效率低:临床级需求下,单批次需获取上亿级细胞,传统培养方案易因细胞增殖速度慢、传代后活力下降,难以满足规模需求;
(2)质量难把控:血清批次差异会导致细胞表型不稳定,长期传代后分化潜能易丢失,且动物源成分的存在,为临床转化埋下安全隐患。
要突破这两大痛点,必须从“培养体系” 入手 ——MCM CulMsc-SFM31 Pro 无血清培养基 + 水溶性微载体(WSCarrier01)的组合,正是为解决这些问题量身打造。
MCM CulMsc-SFM31 Pro无血清培养基:
安全与效能的 “双保障”
作为整个培养方案的“核心引擎”,这款培养基专为脐带来源、胎盘来源、脂肪来源MSC设计,从根源上规避传统血清培养的弊端:
▲ 安全合规:成分完全明确,无血清、无动物源成分,蛋白质含量极低,已完成美国FDA DMF备案,完全符合临床转化对 “安全性” 的严苛要求;
▲ 全流程适配:既能支持原代MSC分离(酶消化法、组织块法均可高效应用),又能实现长期稳定传代,全程维持细胞的分化潜能,避免传代过程中细胞 “丢失分化能力”;
▲ 规模化友好:无需额外添加血清或血清替代物,可直接对接生物反应器,省去“血清驯化” 的繁琐步骤,为后续大规模培养扫清障碍。
水溶性微载体(WSCarrier01):
给细胞打造 “仿生微环境”
三维培养中,细胞的“生长环境” 直接影响增殖效率与活力。这款水溶性微载体通过“精细化仿生设计”,为 MSC 创造接近体内的生长条件:
▲ 结构精准可控:从材料生化组分、二维表面拓扑结构,到三维空间构象、孔隙大小,均经过反复优化,能高效促进MSC 粘附、铺展,为细胞增殖打下基础;
▲ 抗剪切保护:独特的多孔结构可有效缓冲搅拌、通气过程中产生的剪切力,减少细胞损伤—— 要知道,大规模培养中,剪切力导致的细胞死亡,往往是 “量产失败” 的隐形杀手;
▲ 维持表型稳定:仿生环境能更好地保留MSC 的干细胞特性,避免因环境不适导致的表型漂移,确保传代后细胞功能 “不打折扣”。
案例一
原代分离+ 细胞库建立,高效完成 “奠基工作”
◆ 样本信息:新鲜脐带样本
◆ 培养流程:
1)按标准操作分离华通氏胶,将组织块均匀铺在T175 瓶中,加入15mL MCM CulMsc-SFM31 Pro培养基;
2)置于37℃ CO₂培养箱中静置 7 天(期间不移动、不摇晃,避免影响细胞贴壁);
3)第7天首次换液,之后每3天换液一次,第12天细胞融合率达80%时传代,获得P0细胞;
4)P0细胞传代至融合率80%时冻存,建立主细胞库(P1);复苏1支P1细胞(5×10⁶/ 支),传代至P3冻存,建立工作细胞库。
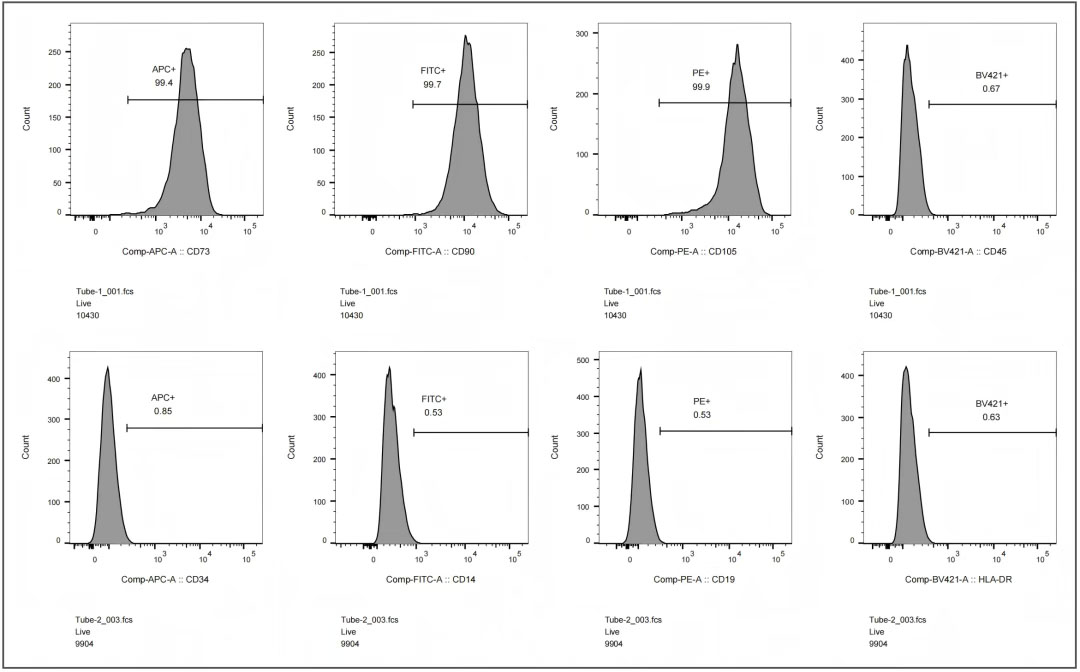
图1. 间充质干细胞流式表征图
数据显示CD73、CD90和CD105阳性率不低于95%;CD45、CD34、CD14、CD19和HLA-DR阳性率不高于2%。
MCM CulMsc-SFM31 Pro从原代分离到细胞库建立,这套方案能高效、稳定完成“前期奠基”,可以有效支持原代细胞分离及细胞库建立,为后续培养提供优质种子细胞。
案例2
连续传代 15 代,增殖与表型 “双稳定”
◆ 样本信息:新鲜P0 细胞
◆ 培养流程:根据不同代次调整接种密度,每72 小时传代一次,从 P0 连续培养至 P15,全程使用 MCM CulMsc-SFM31 Pro 培养基。
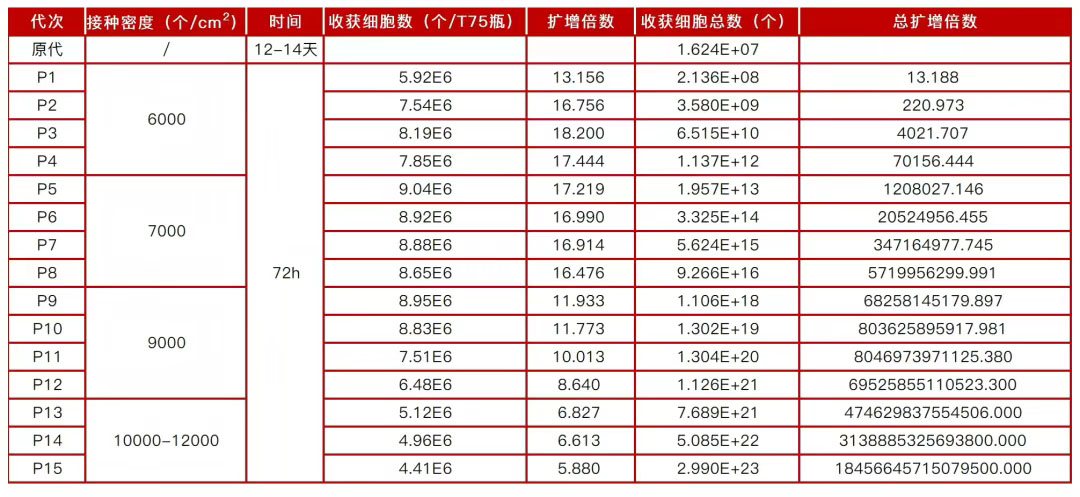
图2. MSC的连续传代培养数据
P1-8,按6-7000cells/cm²接种,72h传代一次,扩增15倍左右。P9-12,按9000cells/cm²接种,72h传代一次,扩增10倍左右。P12-15,按1000-12000cells/cm²接种,72h传代一次,扩增8倍左右
数据显示,即便连续传代至 10 代以上,细胞仍保持高增殖活性与稳定表型,解决了 “长期传代质量下降” 的行业痛点。案例3
3L 玻璃反应器规模培养,对接工业化需求
◆ 样本:冻存P3 细胞
◆ 培养流程:分两组进行反应器培养,均搭配水溶性微载体(WSCarrier01):
1)高密度组:P3 细胞(2×10⁶)起始,先经二维培养扩增至 2×10⁸,再转入 3L 玻璃反应器(P5);
2)低密度组:P3 细胞(2×10⁶)起始,先经二维培养扩增至 6×10⁷,再转入 3L 玻璃反应器(P5)。
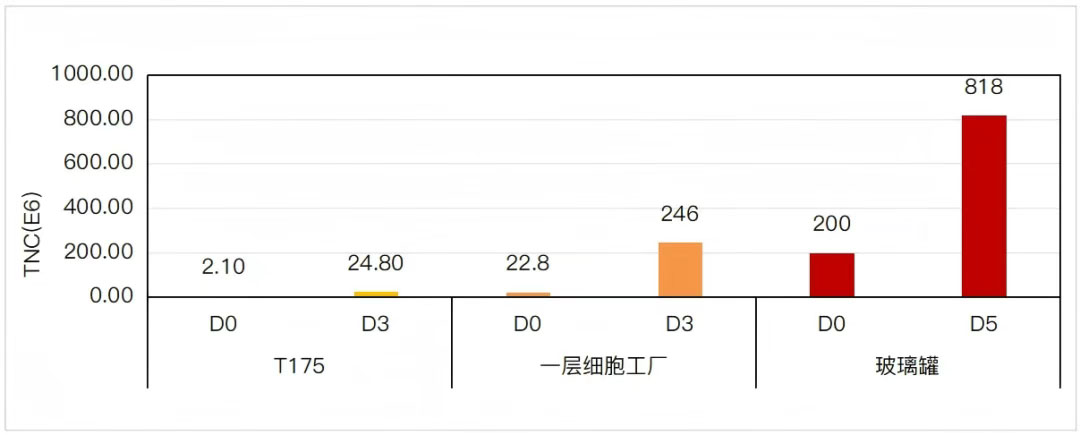
图3. MCM CuIMSC-SFM31 Pro高密图接种MSC培养图
数据显示MCM CuIMSC-SFM31 Pro高密度接种,20E7细胞上玻璃罐培养,共培养5天,收获8.18E8细胞,扩增4.08倍。
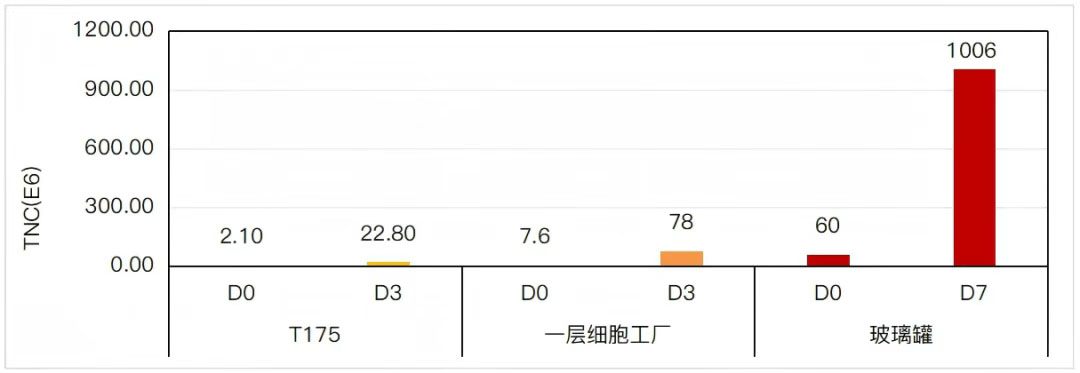
图4. MCM CuIMSC-SFM31低密图接种MSC培养图
数据显示MCM CuIMSC-SFM31低密度接种,6E7细胞上玻璃罐培养,共培养7天,收获10.06E8细胞,扩增16.77倍。
MCM CuIMSC-SFM31 Pro搭配水溶性微载体可以有效支持MSC在玻璃罐反应器上的规模培养,微载体消化酶裂解微载体后检测微载体残留为0.12ug/E7细胞(东富龙配套微载体、裂解液残留检测试剂盒),符合中检院标准<1.5ug>

配套产品清单
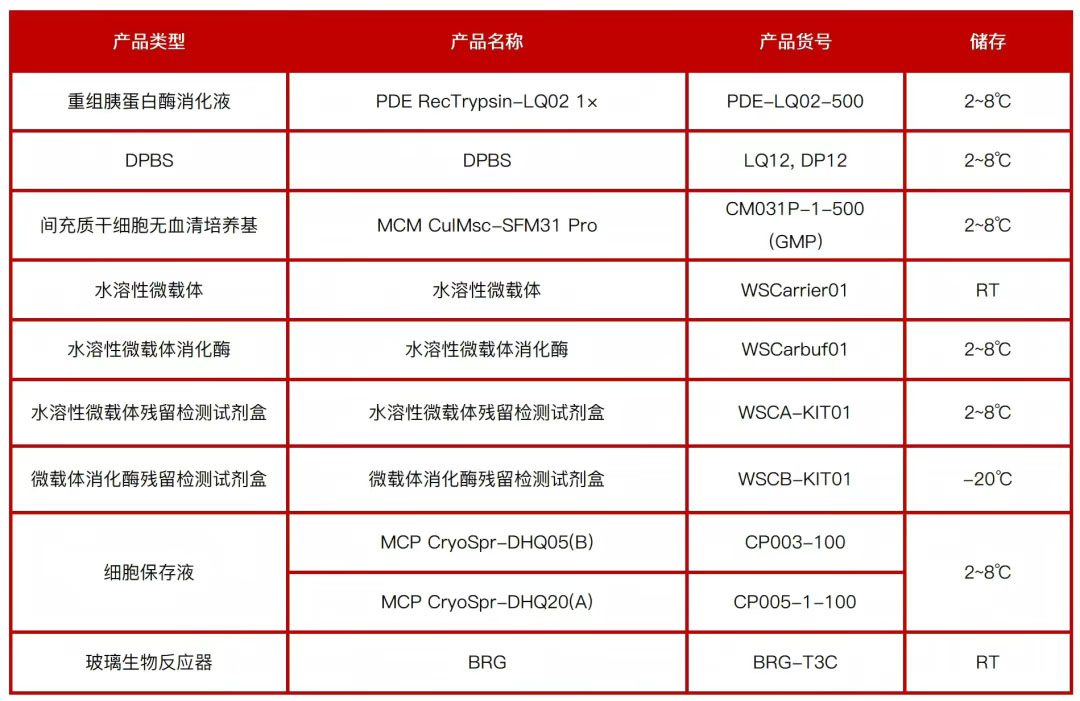
如果需要进一步了解某类来源MSC 的专属培养技巧,或获取方案的详细操作手册,欢迎随时留言咨询!
东富龙生命科学事业部隶属于东富龙集团,目前已全面完成四大关键耗材产品的布局,包括一次性组件、培养基、填料以及过滤器,旨在为广大生物制药和生命科学领域的客户提供量身定制的专业工艺解决方案和耗材技术支持,覆盖从上游细胞培养到下游分离纯化,再到最终的制剂灌装的全工艺链,每一个环节都紧密结合、精准高效,实现了工艺的全流程支持。


