新规下的“合规密码”:东富龙无酚红培养基赋能T细胞培养
- 2026-04-08
- 新闻资讯
- 171
2026年5月,818号令(《生物医学新技术临床研究和临床转化应用管理条例》)、828号令(修订后《中华人民共和国药品管理法实施条例》)将相继正式施行,细胞治疗行业迈入“合规为先”的全新阶段。两大法规为细胞治疗产品划定清晰红线,要求全流程可追溯、质量可控制、风险可防控,尤其对临床级细胞体外培养的原料合规、工艺稳定、检测规范提出严苛标准。
T淋巴细胞(CAR-T、TCR-T、γδT等)的体外扩增质量,直接决定细胞治疗的临床安全性与有效性,而培养基作为细胞生长的“营养基石”,其合规性与性能成为适配新规、实现产业化的核心关键。传统血清培养体系成分复杂、批间差异大、动物源污染风险高,已难以满足新规下的临床申报与产业化需求。
东富龙针对性研发的T淋巴细胞无血清培养基MCM CulLymT-SFM12(A)(无酚红配方),以成分明确、安全高效、适配性广的核心优势,精准契合818/828号令要求,成功助力多家科研机构及企业实现T细胞培养的合规转型与技术突破,成为新规下细胞治疗产业化的优选解决方案。
818/828号令构建起细胞治疗“药品+技术”双轨监管体系,原有培养体系与工艺已无法适配新规要求,成为项目推进的主要阻碍:
合规不达标,申报备案遇阻
含血清培养体系成分未知、来源不可追溯,存在动物源病毒、异种蛋白污染风险,不符合818号令“临床研究用细胞质量安全可控”、828号令“生物制品生产全过程数据可追溯、原料合规可控”的核心要求,无法推进临床申报与技术转化备案。
技术不满足,规模化落地难
为精准适配818/828号令要求,东富龙MCM CulLymT-SFM12(A)(无酚红)从原料、工艺、检测、溯源全维度打造合规培养方案,同时兼顾扩增效率与批间稳定性,一站式破解T细胞培养的合规与技术难题。
成分明确,合规可控
不含动物源成分、无酚红,采用临床级人血白蛋白为原料,蛋白含量低且原料来源可追溯、资质齐全,从源头规避污染风险;无酚红设计避免干扰细胞检测实验,确保检测数据真实准确,契合新规对原料安全与检测合规的双重要求。
配方优化,质量稳定
无需添加血清或血清替代物,可直接用于T细胞无血清培养,大幅降低外源污染风险;配方经多批次验证,有效解决批间差异问题,契合818/828号令“质量均一、稳定可控”的管控标准。
适配性广,赋能规模化
兼容PBMC分离、基因修饰后的多种T细胞亚型培养,支持培养瓶/袋静置培养及一次性生物反应器规模化培养模式;提供1000mL瓶装(适配实验室研发/工艺验证)、2L/5L/10L袋装(适配规模化生产)多规格,完美契合828号令“规模化、标准化生产”导向,助力企业实现从实验室到生产车间的合规转化。
溯源完善,全程可控
建立全流程溯源体系,可提供完整的原料检测报告、生产工艺记录、成品检验报告,实现“从原料到成品”的全程可追溯,完全满足818/828号令“全流程可追溯、全过程可监管”的核心要求。
结合企业现有工艺,东富龙为MCM CulLymT-SFM12(A)(无酚红)制定贴合818/828号令要求的标准化培养流程,无需企业大幅调整现有工艺,每一步操作均可追溯、可验证,大幅降低合规转型成本:
1)PBMC分离与处理:按企业标准及818号令细胞处理规范操作,全程记录参数,确保数据可追溯;
2)细胞接种:T细胞按1~1.5×10⁶/mL密度接种,严格控制接种密度,稳定的激活工艺,保障细胞生长一致性;
3)培养条件控制:37℃、5% CO₂、85%湿度环境,前期静置、后期流加/灌流培养,全程监控并记录环境参数;
4)过程监控与补料:每2天显微观察+细胞计数,按需补加培养基及IL-2,同步记录补料信息;
5)细胞收获与检测:培养14天收获细胞,按新规完成活率、纯度、无菌性等全项检测,留存报告为申报备案提供合规支撑。
同时,东富龙专业应用技术团队全程跟进,提供工艺优化、反应器对接指导、合规培训、申报资料整理等全方位技术支持,加速项目合规落地。
以东富龙MCM CulLymT-SFM12(A)(无酚红)用于T细胞培养为例,经体外扩增,各项指标均达甚至超出企业预期,实现818/828号令全维度合规达标,同时技术性能表现突出:
案例1:复苏冻存的PBMC,静置激活及扩增培养
培养14天,MCMCulLymT-SFM12(A)组细胞总数可扩增132.3倍;培养21天后,MCMCulLymT-SFM12(A)组细胞总数可扩增502倍,对比商业化培养基,存在一定优势。
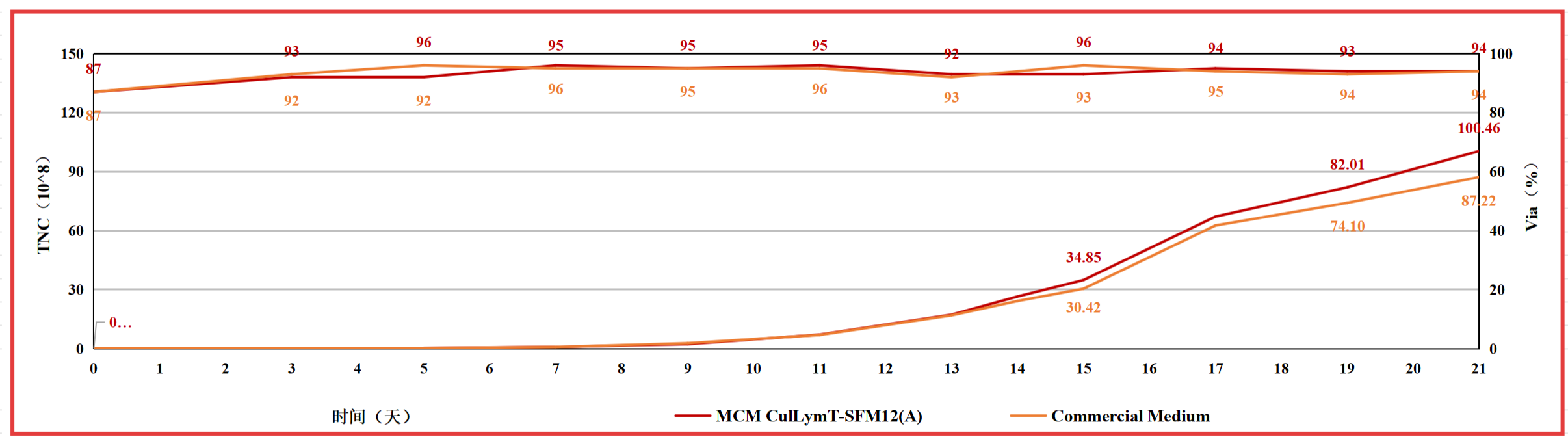
图1. MCM CulLymT SFM12(A)应用于T细胞静置培养--生长曲线
案例2:复苏冻存的PBMC,前期静置激活, 后期反应器灌流扩大培养
前期细胞完成激活培养,达到一定细胞数后进行反应器培养(灌流模式)。共培养8天,MCMCulLymT-SFM12(A)支持细胞总数扩增24.94倍;最高密度达到2.49E7/mL。
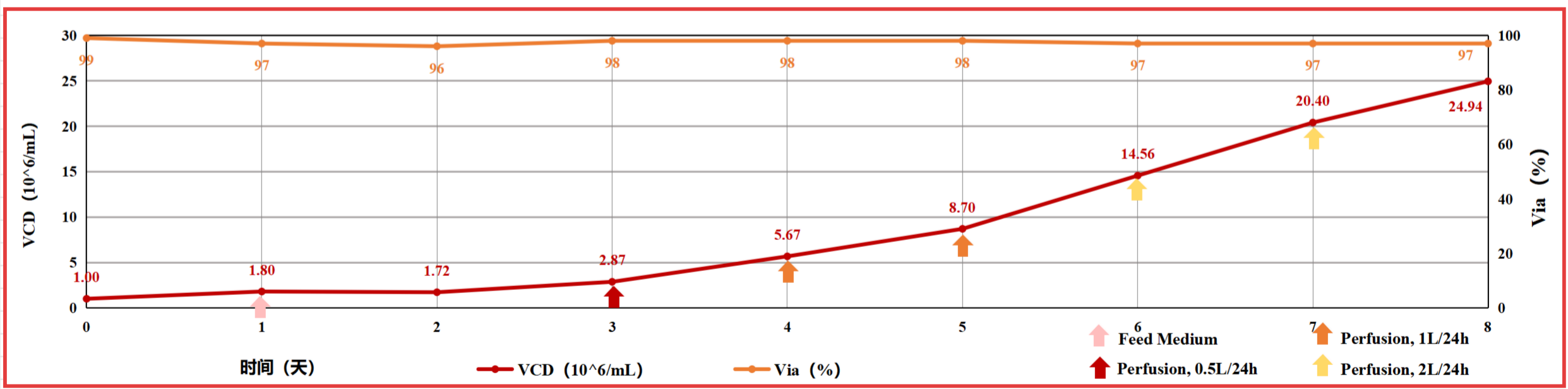
图2.MCM CulLymT SFM12(A) 应用于T细胞反应器培养--SUR10L
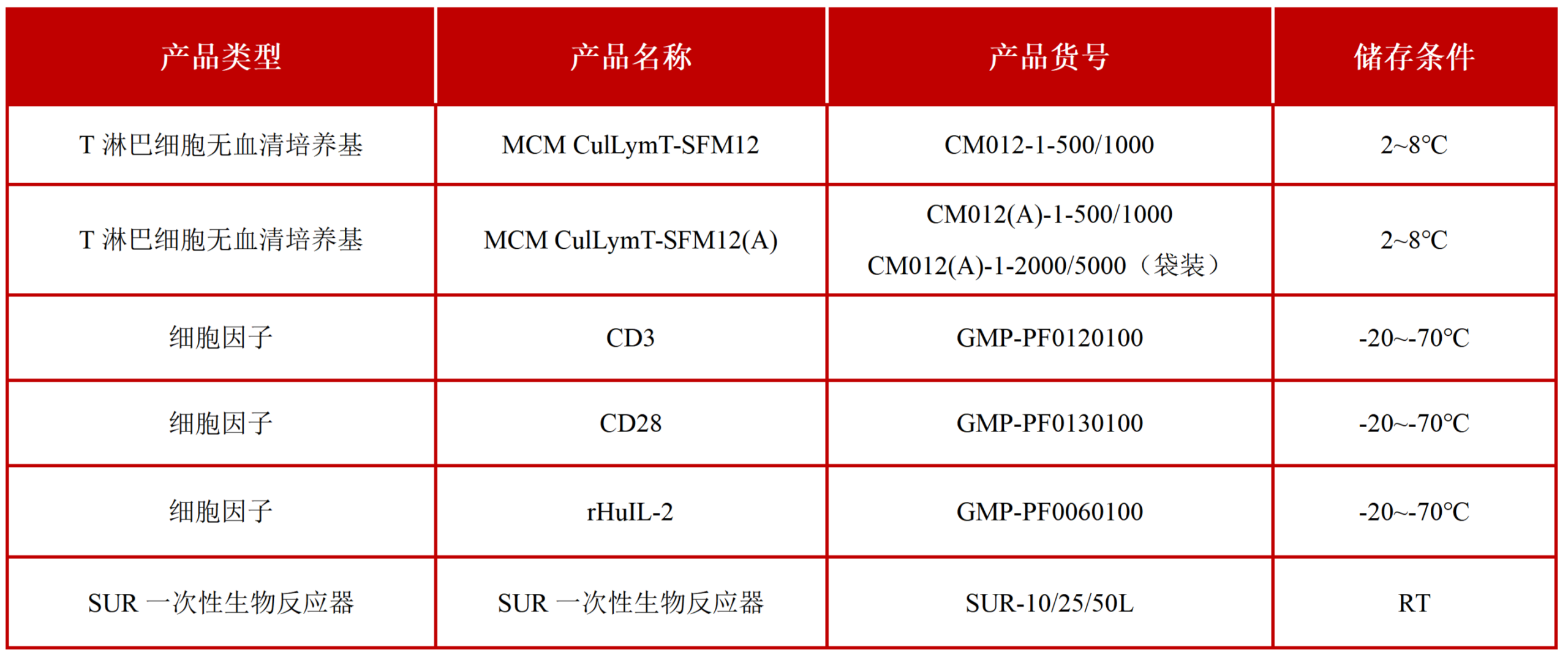
产品信息 818/828号令的落地,不仅为细胞治疗行业划定合规红线,更推动行业从“野蛮生长”向“合规有序”转型,而培养基作为细胞培养的核心原料,其合规性与稳定性直接决定项目备案进度、申报成功率及产业化前景。 东富龙MCM CulLymT-SFM12(A)(无酚红)T淋巴细胞无血清培养基,紧扣两大号令核心要求,以“合规+高效”的产品特性,成功破解T细胞培养的行业痛点,充分体现了东富龙在细胞培养领域的技术实力与合规理念。 未来,东富龙生物试剂将持续深耕细胞治疗领域,紧跟行业法规要求,不断优化产品配方与工艺,研发更多合规、高效、稳定的细胞培养试剂,提供定制化应用支持与全流程合规解决方案,助力更多科研机构及企业突破细胞培养瓶颈,实现合规化、规模化发展,赋能细胞治疗产业化升级,为人类生命健康事业贡献力量! 扫描二维码填写信息,也可拨打电话联系我们,咨询工艺耗材产品或验证服务:64909996-327。 东富龙生命科学事业部隶属于东富龙集团,主要产品包含细胞与基因治疗设备,一次性设备,实验室设备,及四大生物工艺耗材(一次性组件、培养基、填料以及过滤器),旨在为广大生物制药和生命科学领域的客户提供量身定制的专业工艺解决方案和耗材技术支持,覆盖从上游细胞培养到下游分离纯化,再到最终的制剂灌装的全工艺链,每一个环节都紧密结合、精准高效,实现了工艺的全流程支持。